Wenn (neue) Medikamente nicht mehr wirken: Besorgniserregende Ausbreitung multiresistenter Tuberkulose in Mosambik
Mit einer der höchsten Tuberkulose-Inzidenzen (368 Fälle/100.000 Einwohner) in der afrikanischen Region ist Mosambik stark von der Tuberkulose-Epidemie betroffen. Vor allem arzneimittelresistente Tuberkulosefälle stellen eine Herausforderung dar: Schätzungen zufolge traten allein im Jahr 2021 bis zu 4.800 neue Fälle von multiresistenter/Rifampicin resistenter Tuberkulose (MDR-TB, RR-TB) auf. Besonders besorgniserregend sind neue Ergebnisse, die Forschende eines internationalen Konsortiums unter der Leitung des Forschungszentrums Borstel, Leibniz Lungenzentrum nun in der Fachzeitschrift Lancet Infectious Diseases veröffentlichten: Bei den untersuchten MDR-TB-Stämmen wurde ein hoher Anteil an Fluorchinolon- und ein zunehmender Anteil Bedaquilin-Resistenz festgestellt, zwei Schlüsselmedikamente aktueller Therapieschemata zur Behandlung von Patienten mit MDR-TB. Darüber hinaus dokumentierten die Forschenden die Ausbreitung von MDR-TB-Stämmen, deren Rifampicin Resistenz mit den derzeit weltweit eingesetzten molekularen Testverfahren nicht nachgewiesen werden kann.
Eine wirksame Diagnostik und eine effektive Therapie von Patientinnen und Patienten, die an einer multiresistenten Tuberkulose (MDR-TB) erkrankt sind, sind der Schlüssel für eine erfolgreiche Tuberkulose-Bekämpfung. In Mosambik und anderen afrikanischen Ländern hat die Weltgesundheitsorganisation (WHO) den landesweiten Einsatz des molekularen Schnelltest „Xpert MTB/RIF Ultra“ für den MDR-TB Nachweis empfohlen, um eine schnelle MDR-TB-Behandlung im Einklang mit den neuesten Leitlinien der Weltgesundheitsorganisation (WHO) zu ermöglichen.
Für die Behandlung von MDR-TB Erkrankten empfahl die WHO zudem kürzlich ein neues 6-monatiges orales Behandlungsschema (BPaLM), bestehend aus den Antibiotika Bedaquilin, Pretomanid und Linezolid plus Moxifloxacin (bei fehlender Fluorchinolon-Resistenz). Obwohl diese kürzere und besser verträgliche Therapie sehr vielversprechend ist, könnte das nun beschriebene Auftreten von Fluorchinolon- und/oder Bedaquilin-Resistenzen den langfristigen Nutzen gefährden.
In der aktuellen Studie, die von Wissenschaftlerinnen und Wissenschaftlern des Forschungszentrums Borstel, Leibniz Lungenzentrum (FZB) und des Nationalen Gesundheitsinstituts (Instituto Nacional de Saúde, INS, Mosambik) geleitet wurde, setzten die Forschenden modernste Genomsequenzierungstechnologie bei Rifampicin Resistenten (RR) Mycobacterium tuberculosis (Mtb)-Stämmen ein, die zwischen 2015 und 2021 an das Nationale Tuberkulose-Referenzlabor in Maputo übermittelt wurden, um die Übertragung und Entwicklung von arzneimittelresistenten Mtb-Stämmen im Laufe der Zeit zu untersuchen.
Es wurde festgestellt, dass über 20 % der MDR-Mtb-Stämme in Mosambik bereits eine Fluorchinolon-Resistenz aufweisen. Darüber hinaus nimmt die Bedaquilin-Resistenz bei den untersuchten Stämmen stetig zu, von 3 % im Jahr 2016 auf 14 % im Jahr 2021. Die Daten belegen auch eine effiziente Übertragung von MDR-Mtb-Stämmen, besonders von Stämmen mit Fluorchinolon- und/oder Bedaquilin-Resistenzen.
"Die schnelle Resistenzentwicklung und die effiziente Übertragung hochresistenter M. tuberculosis-Stämme stellen eine große Bedrohung für die TB-Kontrolle in Mosambik und den Nachbarregionen dar", sagt Prof. Niemann, Studienkoordinator am FZB und leitender Wissenschaftler am Leibniz-Wissenschaftscampus EvoLUNG, dem Exzellenzcluster "Präzisionsmedizin bei chronischen Entzündungen" (PMI) und dem Deutschen Zentrum für Infektionsforschung (DZIF).
Ebenso besorgniserregend ist die Verbreitung von Mtb-Stämmen mit einer bestimmten Rifampicin-Resistenzmutation (I491F), die mit dem „Xpert MTB/RIF Ultra“ und anderen handelsüblichen molekularen Tests nicht nachgewiesen werden kann. Ein großer Teil dieser I491F-Stämme, auch „diagnostic escape“ Stämme genannt, weist eine weitere Resistenz gegen Bedaquilin oder sogar kombinierte Resistenzen gegen Bedaquilin und Fluorchinolone auf. Der Vergleich mit Stämmen aus Südafrika und Eswatini belegt die grenzüberschreitende Verbreitung von I491F-Stämmen, ein Befund, der dringend weiter untersucht werden muss.
"Angesichts der derzeitigen Diagnosealgorithmen und Behandlungsmethoden kann sowohl die Verbreitung von Rifampicin-Resistenten Stämmen mit I491F-Mutation als auch das vermehrte Auftreten von Bedaquilin-Resistenz die Bemühungen zur Eindämmung der arzneimittelresistenten TB-Epidemie in Mosambik gefährden", so Dr. Sofia Viegas, leitende Wissenschaftlerin und stellvertretende Generaldirektorin des INS.
Die Ergebnisse der Studie werfen grundlegende Fragen zur Entwicklung und Einführung neuer Wirkstoffe und Behandlungsschemata auf. Ohne eine wirksame Diagnostik, eine direkte Umsetzung der Ergebnisse in klinische Entscheidungen und an die Resistenz angepasste Medikamentenregime besteht ein hohes Risiko einer raschen Resistenzentwicklung. Dadurch können auch neu entwickelte Medikamente innerhalb kurzer Zeit unwirksam werden.
Die Studie stellt auch die Rolle molekularer Schnelltests wie der „Xpert MTB/RIF Ultra“ in Regionen in Frage, in denen die Prävalenz von "diagnostic escape" Stämmen hoch ist. Die unkontrollierte Übertragung von MDR-MTB-Stämmen in Mosambik und anderen Teilen Afrikas stellt eine enorme Herausforderung für die Tuberkulosebekämpfung im 21. Jahrhundert dar. Das unterstreicht die Bedeutung einer wirksamen Diagnose und Tuberkuloseüberwachung auf der Grundlage umfassender molekularbiologischer Methoden wie der Sequenzierungstechnologien.
"Diese Themen stehen im Fokus unserer Forschung, die wir in nationalen und internationalen Projekten bearbeiten. Dabei ist die Umsetzung der Ergebnisse aus der Grundlagenforschung in die Anwendung von besonderer Bedeutung,“ erklärt Prof. Niemann.
Über das Forschungszentrum Borstel, Leibniz Lungenzentrum
Das Forschungszentrum Borstel ist das Lungenforschungszentrum der Leibniz-Gemeinschaft. Im Fokus stehen chronisch-entzündliche Lungenerkrankungen wie Asthma, chronisch-obstruktive Lungenerkrankung (COPD) und Allergien, sowie Tuberkulose und andere infektionsbedingte Entzündungen der Lunge. Das übergeordnete Ziel der interdisziplinären Forschungsaktivitäten ist, die Ursachen und Mechanismen chronisch-entzündlicher und degenerativer Erkrankungen der Lunge aufzuklären, um daraus neue innovative Konzepte zu deren Diagnostik, Prävention und Therapie abzuleiten.
Zur Leibniz-Gemeinschaft gehören zurzeit 97 Forschungsinstitute und wissenschaftliche Infrastruktureinrichtungen für die Forschung. Die Ausrichtung der Leibniz-Institute reicht von den Natur-, Ingenieur- und Umweltwissenschaften über die Wirtschafts-, Sozial- und Raumwissenschaften bis hin zu den Geisteswissenschaften. Leibniz-Institute arbeiten strategisch und themenorientiert an Fragestellungen von gesamtgesellschaftlicher Bedeutung. Bund und Länder fördern die Institute der Leibniz-Gemeinschaft daher gemeinsam. Die Leibniz-Institute beschäftigen etwa 20.000 Mitarbeiterinnen und Mitarbeiter bei einem Jahresetat von ca. 2,1 Milliarden Euro. (www.leibniz-gemeinschaft.de)
Wissenschaftlicher Kontakt:
Prof. Dr. Stefan Niemann
Forschungszentrum Borstel, Leibniz Lungenzentrum
Parkallee 1, 23845 Borstel
+49 4537 188-7620
sniemann@fz-borstel.de
Pressekontakt:
Britta Weller
Öffentlichkeitsarbeit
Forschungszentrum Borstel, Leibniz Lungenzentrum
Parkallee 1, 23845 Borstel
+49 4537.188-2870
Fax: +49 4537.188-2600
bweller@fz-borstel.de
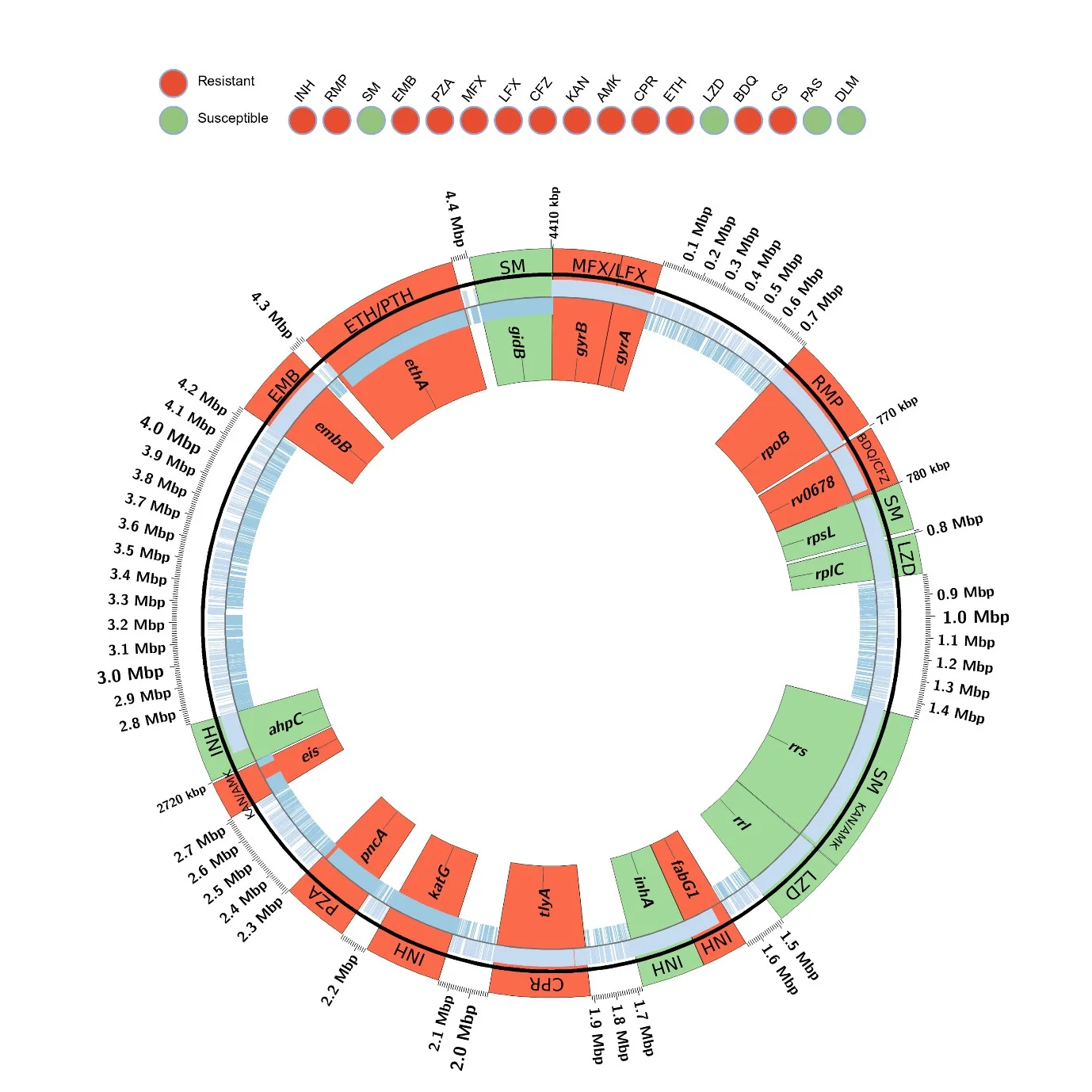
Antibiotika Resistenz Profil eines klinischen Mycobacterium tuberculosis Stamms aus Mosambik, welches mittels Gesamtgenom-Sequenzierung bestimmt wurde. Die farbigen Flächen zeigen im inneren Ring den Gennamen der Genom-Abschnitte (Vergrößerung 500x), die auf Resistenzmutationen überprüft wurden und auf dem äußeren Ring das betroffene Antibiotikum. An dem äußeren Ring wird die genomische Position in Millionen Basenpaaren (Mbp) angezeigt. Grün: Sensitiv, Rot: Resistent. INH: Isoniazid; RMP: Rifampicin; SM: Streptomycin; EMB: Ethambutol; PZA: Pyrazinamid; MFX/LFX: Fluorquinolone; CFZ: Clofazimin; KAN: Kanamycin; AMK: Amikacin; CPR: Capreomycin; ETH: Ethionamid; LZD: Linezolid; BDQ: Bedaquilin; CS: Cycloserin; PAS: Paraaminosalicylsäure; DLM: Delamanid.
Originalpublikation:
Emergence of bedaquiline resistant tuberculosis and of multidrug-resistant and extensively drug-resistant Mycobacterium tuberculosis strains with rpoB Ile491Phe mutation not detected by Xpert MTB/RIF in Mozambique: a retrospective observational study. Barilar et al., The Lancet Infectious Diseases
DOI: https://doi.org/10.1016/S1473-3099(23)00498-X
Über den Exzellencluster PMI
Der Exzellenzcluster „Präzisionsmedizin für chronische Entzündungserkrankungen/Precision Medicine in Chronic Inflammation“ (PMI) wird von 2019 bis 2025 durch die Exzellenzstrategie des Bundes und der Länder gefördert (ExStra). Er folgt auf den Cluster Entzündungsforschung „Inflammation at Interfaces“, der bereits in zwei Förderperioden der Exzellenzinitiative (2007-2018) erfolgreich war. An dem neuen Verbund sind rund 300 Mitglieder in acht Trägereinrichtungen an vier Standorten beteiligt: Kiel (Christian-Albrechts-Universität zu Kiel, Universitätsklinikum Schleswig-Holstein, Muthesius Kunsthochschule, Kiel Institut für Weltwirtschaft (IfW) und Leibniz-Institut für die Pädagogik der Naturwissenschaften und Mathematik), Lübeck (Universität zu Lübeck, Universitätsklinikum Schleswig-Holstein), Plön (Max-Planck-Institut für Evolutionsbiologie) und Borstel (Forschungszentrum Borstel - Leibniz Lungenzentrum).
Ziel ist es, die vielfältigen Forschungsansätze zu chronisch entzündlichen Erkrankungen von Barriereorganen in ihrer Interdisziplinarität verstärkt in die Krankenversorgung zu übertragen und die Erfüllung bisher unbefriedigter Bedürfnisse von Erkrankten voranzutreiben. Drei Punkte sind im Zusammenhang mit einer erfolgreichen Behandlung wichtig und stehen daher im Zentrum der Forschung von PMI: die Früherkennung von chronisch entzündlichen Krankheiten, die Vorhersage von Krankheitsverlauf und Komplikationen und die Vorhersage des individuellen Therapieansprechens.
Pressekontakt:
fbuhse@uv.uni-kiel.de0431/880 4682 https://precisionmedicine.de
Exzellenzcluster „Präzisionsmedizin für chronische Entzündungserkrankungen“
Wissenschaftliche Geschäftsstelle
Leitung: Dr. habil. Susanne Holstein
Christian-Albrechts-Platz 4, D-24118 Kiel
Sonja Petermann
0431/880-4850, Telefax: 0431/880-4894
spetermann@uv.uni-kiel.de
Twitter: PMI @medinflame