Allergische Reaktionen gezielt abschwächen
Bestimmte Untergruppen von IgG-Antikörpern im Blut können allergische Reaktionen ausbremsen
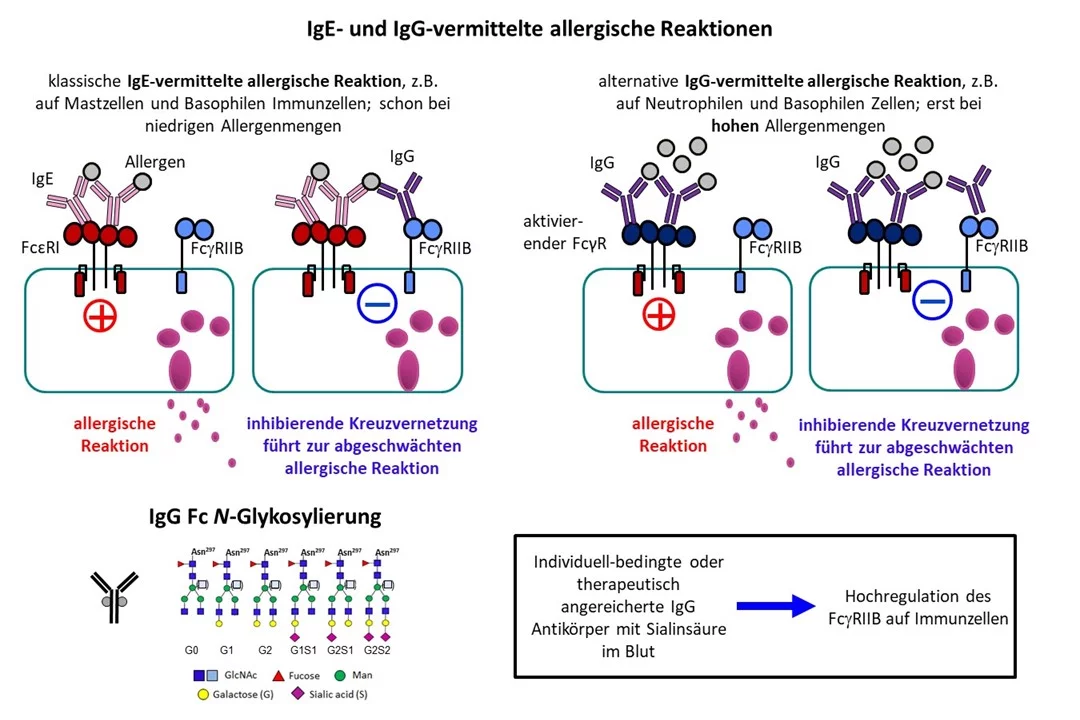
Bei einer allergischen Reaktion binden typischerweise Allergene wie etwa Gräserpollen oder Hausstaubmilben an spezifische Antikörper des Typs IgE. Der IgE-Antikörper aktiviert daraufhin einen Rezeptor auf bestimmten Immunzellen, den sogenannten Mastzellen und Basophilen, z.B. in der Haut oder den Schleimhäuten. Das löst die Ausschüttung von Entzündungsmediatoren wie Histamin aus. Diese sorgen für die bekannten Symptome: Es kommt zur Rötung und Schwellung der Haut oder Schleimhaut, sowie Juckreiz und einer vermehrten Schleimbildung in den Schleimhäuten.
Diese durch die IgE-Antikörper vermittelte allergische Reaktion kann durch Allergen-spezifische Antikörper des Typs IgG reduziert werden. Solche Allergen-spezifischen IgG-Antikörper werden von Allergikern oft selbst gebildet und können durch eine gezielte Allergen-spezifische Immuntherapie weiter erhöht werden. Die Verminderung der IgE-vermittelten allergischen Reaktion kann dann auf zwei verschiedenen Wegen erfolgen: Zum einen binden IgG-Antikörper direkt an das Allergen und blockieren damit die Bindung des Allergens an die IgE-Antikörper, man spricht dann von einer Allergenmaskierung. Im zweiten Fall verbinden die IgG Antikörper über das Allergen den Rezeptor, an den der IgE Antikörper auf Mastzellen oder Basophilen bindet, mit einem hemmenden IgG-Rezeptor, den FcγRIIB. Dies wird als inhibierende Kreuzvernetzung bezeichnet und verhindert die Aktivierung der Immunzellen und damit die IgE-vermittelte allergische Reaktion.
Neben der klassischen IgE-vermittelten allergischen Reaktion gibt es immer mehr Hinweise dafür, dass bei hohenAllergendosen auch IgG Antikörper allergische Reaktionen auslösen können, zum Beispiel bei allergischen Reaktionen gegen Medikamente. Dabei binden die IgG-Antikörper an aktivierende Fcγ Rezeptoren z.B. auf Neutrophilen und Basophilen Immunzellen. Auch diese IgG-vermittelte Immunreaktion wird durch eine inhibitorische Kreuzvernetzung über den inhibitorischen FcγRIIB kontrolliert.
Ein Forschungsteam unter Beteiligung von Mitgliedern des Exzellenzclusters „Precision Medicine in Chronic Inflammation“ (PMI) hat nun herausgefunden, wie man diesen Mechanismus der inhibierenden Kreuzvernetzung gezielt ausnutzen kann, um eine IgE- als auch eine IgG-vermittelte allergische Reaktion abzuschwächen. Ihre Ergebnisse haben Janina Petry und Lara Dühring aus der Arbeitsgruppen für Immunologie und Glykoanalytik von PMI-Mitglied Professor Marc Ehlers am Institut für Ernährungsmedizin (IEM) und Johann Rahmöller von der Klinik für Anästhesiologie und Intensivmedizin an der Universität zu Lübeck nun in der Fachzeitschrift The Journal of Allergy and Clinical Immunology veröffentlicht.
Je mehr inhibitorische FcγRIIB-Rezeptoren desto schwächer die allergische Reaktion
„Wir haben angenommen, dass die IgE-vermittelte als auch eine IgG-vermittelte allergische Reaktion umso stärker abgeschwächt wird, je mehr es von diesen hemmenden FcγRIIB-Rezeptoren auf den Immunzellen gibt. Daher haben wir nach Mechanismen gesucht, die dazu führen, dass möglichst viel FcγRIIB auf Immunzellen exprimiert wird“, erklärt Prof. Marc Ehlers.
In vorhergehenden Untersuchungen hatten Forschende beobachtet, dass bei Patientinnen und Patienten mit entzündlichen Autoimmunerkrankungen unter einer bestimmten Therapie der FcγRIIB-Rezeptor häufig vermehrt auf bestimmten Immunzellen auftritt. Bei Autoimmunerkrankungen richtet sich das Immunsystem gegen Bestandteile des eigenen Körpers und führt so zu Entzündungen, während bei Allergien das Immunsystem auf eigentlich ungefährliche Fremdkörper wie Gräserpollen reagiert.
„Patientinnen und Patienten mit Autoimmunerkrankungen werden oft mit großen Mengen an IgG-Antikörpern aus dem Blut von gesunden Spendern behandelt, dem sogenannten IVIg, intravenöses Immunglobulin“, erklärt Professor Ehlers. „2006 haben Forschende gezeigt, dass in dieser IgG Antikörper-Mischung eine Untergruppe von IgG Antikörpern dazu führt, dass bei den Behandelten mehr inhibitorischer FcγRIIB auf bestimmten Immunzellen gebildet wird, wodurch eine IgG-Autoantikörper-vermittelte Autoimmunreaktion abgeschwächt wird. Diese Beobachtung bildet die Grundlage für unsere Arbeit“, so Ehlers weiter. Die entscheidende Untergruppe besteht aus IgG-Antikörpern, die an ihrem sogenannten Fc-Teil, einen bestimmten Zucker-Baustein, die Sialinsäure, tragen. Diese Antikörper binden an Rezeptoren, deren ausgelöste Signalkaskade am Ende dazu führt, dass auf Immunzellen mehr von dem hemmenden FcγRIIB Rezeptor gebildet wird.
Bestimmte IgG Antikörper führen zu mehr inhibitorischen Rezeptoren auf Immunzellen
„In unserer Arbeit haben wir nun in Allergie-Experimenten gezielt den Anteil von Allergen-unspezifischen IgG-Antikörpern mit Sialinsäure im Blut erhöht“, erklärt Prof. Ehlers. „Dadurch wurde auf den Immunzellen mehr von dem entscheidenden FcγRIIB Rezeptor gebildet, wodurch die allergischen Reaktionen abgeschwächt werden konnten“, so Ehlers weiter.
Wieviel IgG-Antikörper mit Sialinsäure im Blut gesunder Menschen von Natur aus zirkulieren, variiert sehr stark zwischen den Individuen. Das Forschungsteam konnte in einer ersten Untersuchung zeigen, dass Menschen mit einem höheren Anteil der IgG-Antikörper mit Sialinsäure im Blut auch mehr von dem FcγRIIB Rezeptor auf Immunzellen bilden. „Die Daten deuten darauf hin, dass Allergikerinnen und Allergiker aufgrund ihres individuellen Anteils an IgG Antikörpern mit Sialinsäure im Blut eine allergische Reaktion unterschiedlich gut ausbremsen können.“
„Die Beobachtungen helfen uns genauer zu verstehen, welche Rolle die sogenannte Glykosilierung der IgG-Antikörper, also die biochemischen Zuckerbausteine am Fc-Teil von IgG-Antikörpern, bei allergischen Reaktionen spielen“, sagt Ehlers. „Diese Erkenntnisse könnten zukünftig dabei helfen, Therapien zu entwickeln, die gezielt zu einer vermehrten Bildung des hemmenden Rezeptors FcγRIIB auf den Immunzellen führen und so eine allergische Reaktion abschwächen“, so Ehlers weiter.
Kontakt:
Prof. Dr. rer. nat. Marc Ehlers
Institut für Ernährungsmedizin
Universität zu Lübeck und Universitätsklinikum Schleswig-Holstein, Campus Lübeck
0451/3101-8410
Marc.Ehlers@uksh.de
Bestimmte Untergruppen von IgG Antikörpern im Blut können allergische Reaktionen ausbremsen, das hat ein Forschungsteam unter Beteiligung von PMI-Mitglied Prof. Marc Ehlers der Universität zu Lübeck und es UKSH, Campus Lübeck, gezeigt.
Sowohl die IgE- als auch die IgG-vermittelte allergische Reaktion kann durch Allergen-spezifische Antikörper des Typs IgG reduziert werden - durch inhibierende Kreuzvernetzung. Ein Forschungsteam unter Beteiligung von Mitgliedern des Exzellenzclusters „Precision Medicine in Chronic Inflammation“ (PMI) hat nun herausgefunden, wie man diesen Mechanismus der inhibierenden Kreuzvernetzung gezielt ausnutzen kann, um eine IgE- als auch eine IgG-vermittelte allergische Reaktion abzuschwächen.
Originalpublikation:
Petry J*, Rahmöller J*, Dühring L*, Lilienthal G-M, Lehrian S, Jana Sophia Buhre, Bartsch YC, Epp A, Lunding H, Moremen KW, Leliavski A, and Ehlers M. Enriched blood IgG sialylation attenuates IgG-mediated and IgG-controlled-IgE-mediated allergic reactions. J Allergy Clin Immunol 2020; doi: 10.1016/j.jaci.2020.05.056.
*diese Autoren trugen in gleichem Maße zur Publikation bei.
Über den Exzellencluster PMI
Der Exzellenzcluster „Präzisionsmedizin für chronische Entzündungserkrankungen/Precision Medicine in Chronic Inflammation“ (PMI) wird von 2019 bis 2025 durch die Exzellenzstrategie des Bundes und der Länder gefördert (ExStra). Er folgt auf den Cluster Entzündungsforschung „Inflammation at Interfaces“, der bereits in zwei Förderperioden der Exzellenzinitiative (2007-2018) erfolgreich war. An dem neuen Verbund sind rund 300 Mitglieder in acht Trägereinrichtungen an vier Standorten beteiligt: Kiel (Christian-Albrechts-Universität zu Kiel, Universitätsklinikum Schleswig-Holstein, Muthesius Kunsthochschule, Kiel Institut für Weltwirtschaft (IfW) und Leibniz-Institut für die Pädagogik der Naturwissenschaften und Mathematik), Lübeck (Universität zu Lübeck, Universitätsklinikum Schleswig-Holstein), Plön (Max-Planck-Institut für Evolutionsbiologie) und Borstel (Forschungszentrum Borstel - Leibniz Lungenzentrum).
Ziel ist es, die vielfältigen Forschungsansätze zu chronisch entzündlichen Erkrankungen von Barriereorganen in ihrer Interdisziplinarität verstärkt in die Krankenversorgung zu übertragen und die Erfüllung bisher unbefriedigter Bedürfnisse von Erkrankten voranzutreiben. Drei Punkte sind im Zusammenhang mit einer erfolgreichen Behandlung wichtig und stehen daher im Zentrum der Forschung von PMI: die Früherkennung von chronisch entzündlichen Krankheiten, die Vorhersage von Krankheitsverlauf und Komplikationen und die Vorhersage des individuellen Therapieansprechens.
Pressekontakt:
fbuhse@uv.uni-kiel.de0431/880 4682 https://precisionmedicine.de
Exzellenzcluster „Präzisionsmedizin für chronische Entzündungserkrankungen“
Wissenschaftliche Geschäftsstelle
Leitung: Dr. habil. Susanne Holstein
Christian-Albrechts-Platz 4, D-24118 Kiel
Sonja Petermann
0431/880-4850, Telefax: 0431/880-4894
spetermann@uv.uni-kiel.de
Twitter: PMI @medinflame